
本文为节选内容
如需更多报告,联系客服
或扫码获取报告

硫化锂为固体粉末,CAS 号为12136-58-2,锂溶于水时放热,同时发生水解反应,如生成硫氢化锂和氢氧化锂,进一步水解会生成硫化氢。硫化锂在常温下会被氧气缓慢氧化,生成黄色的单质硫和氧化锂;在300℃以上会被氧气氧化生成硫酸锂。硫化锂粉体有较强的吸湿性,即使空气中的微量水分也能引起硫化锂的水解反应,生成有毒的硫化氢气体,大量的硫化锂暴露于含湿空气中,如无特殊防护措施,安全风险极大。因此硫化锂的生产、应用、运输与储存需要重点关注安全性,特别是预防硫化氢溢出带来的潜在风险。
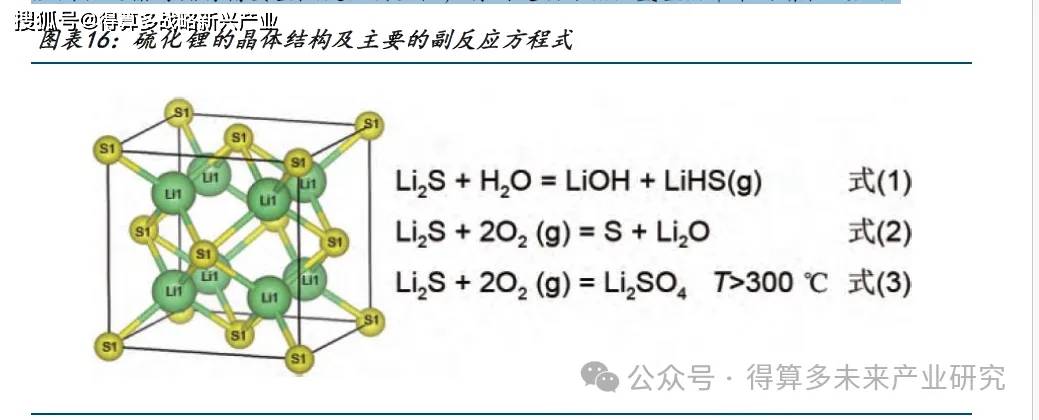
硫化锂的纯度直接制约后续硫化物固态电解质的合成工艺及产物性能。硫化锂中的杂质以
无机锂盐杂质、碳杂质、金属元素杂质以及水分杂质等为主,而硫化锂的产品指标中纯度
参数尤为关键,对硫化物电解质的制备有重要影响;
硫化物固态电解质的高性能高度依赖精确的化学计量比,在材料制备过程中,硫化锂中残留的惰性锂盐杂质(如氧化锂、碳酸锂)在高温固相合成过程中引发化学计量偏差,导致非离子传导性杂相(如Li3PO4 等)的生成。此类杂相在电解质晶界处选择性富集,恶化颗粒界面离子传输动力学,显著降低材料本征离子导率;
部分工艺制备的硫化锂中可能存在的残碳、金属元素等杂质,会升高所制备硫化物电解质的电子电导,导致固态电解质材料在应用中存在较高的漏电流,在电池运行中易于引发电解质分解甚至内部局部锂沉积,进而造成电池内部软短路等问题;
硫化锂的水分残留会引发储存过程中的自发性水解反应,导致材料纯度显著劣化,严重影响硫化物固态电解质材料的可控制备。综上所述,硫化锂的高纯度是实现硫化物固态电解质高性能的重要基础,目前行业内评价硫化锂产品水平主要聚焦白度、物相纯度、多硫含量、水分含量,以及碳杂质含量等角度。

在制备硫化锂时,锂源和硫源的选择具有显著多样性。
硫源:呈负价态的硫离子(S2−)具有本征高反应活性,在传统工业领域中,被广泛用
作高效硫化试剂,如硫化氢,二硫化碳等。这类活性硫源一般可直接与氢氧化锂、碳
酸锂以及有机锂盐等稳定锂盐反应生成硫化锂。而硫单质或更高价态的硫前体需经
历还原过程,借助还原剂如氢化锂等还原性锂盐、金属锂单质等直接反应生成硫化锂。
锂源:锂源可分为两种,一种是强还原性锂源(金属锂或有机锂类),参与硫源的氧化
还原反应;另一种是惰性锂源(如氢氧化锂等传统锂盐),仅作为锂供体,不参与氧化
还原反应。如前文所述,前者一般可和单质硫直接反应生成硫化锂;后者一般需要和
高活性硫化剂,如硫化氢,二硫化碳等进行反应。具有双功能前体特性如硫酸锂能够
同时提供锂源和硫源,通过碳热、镁热、铝热等除氧工艺实现硫价态调控,直接得到
硫化锂。
(1)高活性锂/硫源工艺:原料贵,安全风险较大,不利于规模化生产优势:有较高的反应活性以及良好的产物收率。由于锂/硫源的反应活性高,无需外界提供苛刻条件促进反应进行,同时工艺路线对应的基础化学反应简单,不易产生副产物,从而产物纯度高。目前市场中的高纯硫化锂产品也多来自此工艺路线。缺陷在于:成本昂贵+较大安全风险。其自身活性高,不宜保存,成本也相比稳定锂/硫源更为昂贵;不仅如此,高活性反应物除了自身会带来安全风险,其反应进程往往剧烈,不易控制,整个反应路线也有较大安全风险。
①锂硫化合工艺:由于还原性有机锂盐的成本高昂,且锂含量低,应用强还原性有机锂盐(如叔丁基锂、硼氢化锂、萘锂等)的制备工艺一般用于合成纳米化硫化锂正极材料,不适用于硫化锂量产。金属锂或氢化锂本身锂含量高,而且具有极高的反应活性,一般和单质硫直接进行反应,生成的硫化锂不仅白度极高(蓝光白度>83%),且几乎不引入其他杂质,纯度可达到99.9%以上,是目前百克级高纯硫化锂制备的优选方案之一。
②H2S 中和工艺。应用硫化氢制备硫化锂源自硫化氢与氢氧化锂的中和反应,工艺简洁路线。通过原位转化H2S 为Li2S,不仅实现危废减排,同时可以大幅提高H2S 的产业附加值,因此该路线适用于油气田等H2S 富集区的原位转化,可有效规避H2S 跨区域运输风险。但原料地理依赖性(需匹配H2S 气源)导致工艺普适性受限,加之水解副反应抑制技术尚未成熟,致使产业化进程滞后。
(2)化学稳定锂/硫源工艺:原料便宜,过程安全,适合规模化当前硫化锂规模合成技术存在三条典型路径,其共性特征表现为:①原料廉价且较为易得;
②大气环境耐受性优异,投料端无须严格环境管控;③工艺过程本征安全。应用稳定锂/硫源的温和反应路线有利于进一步工艺降本和规模化。
水合肼还原工艺:高效低成本,但要求反应控制精确原理:在碱性介质中,单质硫于热驱动条件下易发生价态歧化反应,硫元素的歧化倾向导致高价硫物种难以彻底清除,终产物仍存在Li2SO3、Li2S2O3 等伴生杂质,引入水溶性还原助剂(如水合肼)可显著降低体系氧化势,促使反应平衡向硫负离子(S2−)方向迁移。有研究通过引入水合肼作为液相还原介质,使硫单质与氢氧化锂在常温下即可完成前体合成,经后续梯度热处理(400~600℃)促进硫物种完全还原,最终获得纯度≥99.95%的Li2S 粉体。
优势:该工艺创新性地利用强还原剂将S 原位转化为S2−,进而和廉价锂盐,如氢氧化锂或碳酸锂,直接反应形成高效、低成本的硫化锂制备工艺路线。劣势:需要较为精确的反应控制,如果反应控制不当,水合肼将硫单质还原的过程中极易产生大量的中间产物多硫化锂(Li2Sx),水合肼属于管制危险品,同时对人体及环境具有毒性,工程化实施需同步构建封闭式操作单元与完备防护体系。
液相复分解工艺:原料便宜,易于规模化,但提纯成本高原理:硫化钠和廉价锂盐可通过复分解路经生成硫化锂,Li2S 在乙醇中呈现可溶性,但卤化钠、硝酸钠等盐类难溶于乙醇,该溶解特性差异构成Na2S 与锂盐发生复分解反应的核心驱动力。
优势:①原料成本低廉且来源广泛;②该反应体系表现出优异的动力学特性,在室温下即实现硫化锂可控合成;③液相工艺可结合自动化产线,有望实现规模化连续化生产。
劣势:①通过液相法制备硫化锂,后续均需增加中高温热处理来脱除有机溶剂以及水分,抵消了低温复分解反应本应有的节能优势;同时低温下生成的小粒径硫化锂因热处理过程出现晶粒粗化,降低其应用时的反应活性;②涉及大量溶剂的循环使用,溶剂安全性以及溶剂中的水氧含量均需严格控制,以满足生产过程品控要求;③市售硫化钠原料的纯度不足,作为反应原料需要二次提纯;④复分解反应的副产物不易完全去除,仍需增加额外提纯工步,在长期储存过程中,残留水分诱导硫化锂的分解,需设计针对性抑制策略。
(1)纯度:由于原料的高活性、高纯度,锂硫化合工艺性能突出。
硫化锂产品质量呈现以下规律性特征:①应用高活性锂/硫源的反应路线反应过程简洁,机理明确,其产物收率及纯度指标在现有方法中表现最优。②液相合成路线受限于溶剂脱除工序,此类路线生产的硫化锂产品易于出现溶剂残留、水分以及多硫杂质超标等问题,而用于脱除此类杂质而增加的中高温除杂工艺可能引发溶剂碳化,引入新的杂质。③原料安全性高的工艺路线多依赖高温还原反应,而硫元素的价态复杂,反应路径多,副反应难以根除,此类工艺路线制备的硫化锂产品常含无机锂盐、残碳等杂质,一般需结合二次提纯工艺提升纯度。
(2)安全性:碳热还原法(固相法)、液相法的安全性更优,适合规模化生产。硫化锂制备工艺的安全风险主要源自原料活性、制备过程、辅助化学品。①原料活性:高活性硫源,如硫化氢原料具有剧毒;高活性锂源,如金属锂、氢化锂及有机锂盐极易燃爆;
②反应过程:氢化锂和单质硫反应释放大量氢气、金属锂或有机锂与单质硫反应的剧烈放热等特性显著提升了防火防爆与毒害防护的工程复杂度;③工艺辅助体系:用于还原硫酸锂的金属粉末或氢气、可溶解金属锂的液氨、用于还原单质硫的水合肼,以及用于支持复分解反应进行的NMP(N-甲基吡咯烷酮)等均需建立专项防护机制。高纯度硫化锂制备工艺往往伴随安全边际成本的显著增加。
(3)经济性:碳热还原法、水合肼还原法、液相复分解法均有潜力。
成本分析揭示关键规律:原材料在产业链中的前体属性越显著(如硫酸锂处于锂盐加工前端),其市场价格传导效应越弱,对应工艺的单位质量硫化锂原料成本呈现梯度递减特征。当前硫化锂主流制备工艺仍处于产业化验证阶段,其规模经济性尚未完全显现。碳热还原路线展现出显著经济性优势,主要归因于硫酸锂的低价特性及其作为碳酸锂上游前体的产业定位优势;硫化氢中和工艺和水合肼还原工艺的原料成本构成类似,均主要源于锂源,在锂盐价格趋于稳态的市场环境下,进一步降本需依赖工艺改进;复分解工艺的核心原料若用水合硫化钠,价格会高于水合肼法,但存在LiOH+H2S 的搭配方案,价格会更低;锂硫化合工艺由于使用了价格高昂的金属锂,所以锂硫化合工艺的原料成本远高于其他工艺。