
合成生物学的发展脉络分析(附30页报告)
本文为节选内容
如需更多报告,联系客服
或扫码获取报告

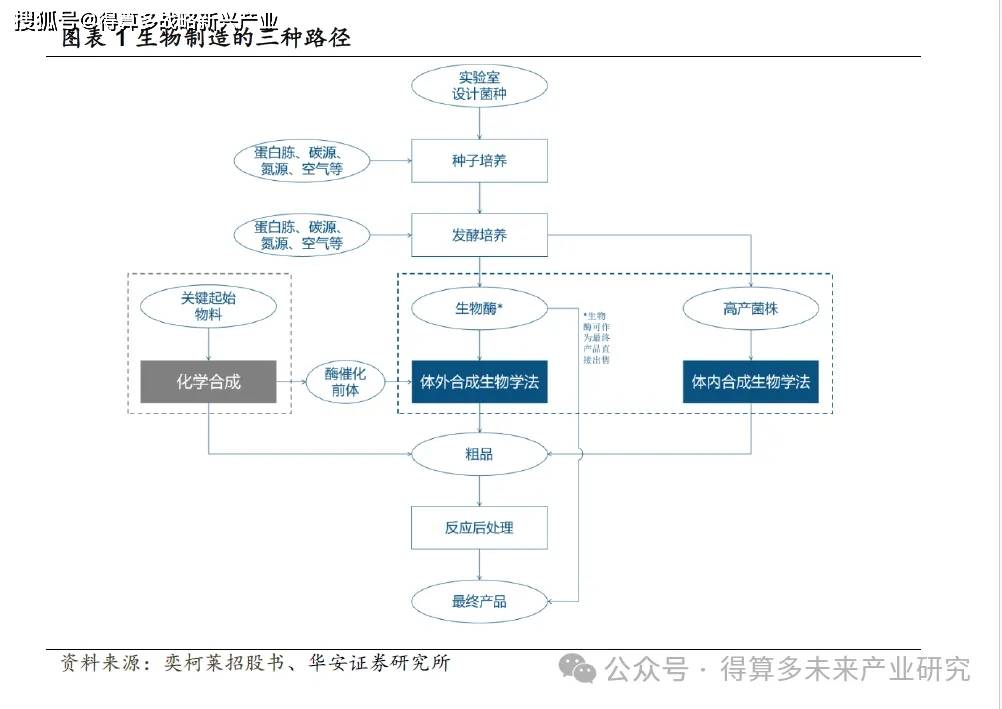
合成生物学是一门基于工程化的设计理念,结合生物学、化学、医学、农学、工程学、计算机与数据科学等交叉学科技术,旨在设计和构建新的生物系统,以实现特定的功能。合成生物学本质是让细胞为人类工作生产想要的物质,秉持系统生物学“自上而下”的“分析”理念设计细胞工厂,结合“自下而上”的“建造”理念构建细胞工厂,形成闭环的正向工程 。针对特定需求,合成生物学将运用微生物细胞工厂构建技术、微生物高效合成化学品的代谢调控机制、无细胞合成技术等主要技术工具,设计构建元器件或模块,通过这些元器件对现有自然生物体系进行改造和优化,或者设计合成全新可控运行的人工生物体系,最终满足需求。在实际生产路径上,合成生物学工艺主要包括以生物酶催化为核心的体外合成生物学法、以微生物细胞工厂为核心的体内合成生物学法,以及利用合成生物学技术优化部分原路径的化学合成法。
合成生物学与传统发酵工程、基因编辑技术的区别
合成生物学和发酵工程的区别在于合成生物学可以对细胞进行定向性干预,将被动筛选转为主动设计,大幅提升细胞工厂代谢效率、更高效地生产目标物质。发酵反应是通过对微生物(或动植物细胞)进行大规模的生长培养,使之发生化学变化和生理变化,从而产生和积累大量所需要的代谢产物的过程。与传统的微生物发酵相比,合成生物学技术加入后的进步之处在于它可以使代谢过程从反向工程优化到正向工程,不再培养大量菌种并筛选、以期获得高效生产细胞工厂,而是从需求入手,通过对代谢路径的重塑和工程化,直接改造细胞工厂,使底盘生物实现其特定的生物学功能。
合成生物学为传统发酵提供了工程化、模块化、标准化的工具,提高了传统发酵的能力圈。在传统的发酵过程中,人们对细胞的认识比较有限、通过细胞功能确定生产产品,后续产品优化则主要来源于对菌种进行改造或大量筛选,进而研究DNA、蛋白和代谢物对提升产品性能的影响。合成生物学出现后,人们可以对生物元件进行定性和定量,以此为基础重新组装元件,创造新功能。合成生物学的引入大大提高了传统发酵的能力圈,不仅可以利用相对简单的方法提高产品的质量和生产效率,还能生产原本不能生产或原本效率低下的产品。
合成生物学的主要工具包括微生物细胞工厂构建技术、微生物高效合成化学品的代谢调控机制、无细胞合成技术。微生物细胞工厂(microbial cell factories,MCFs)是绿色生物制造的核心环节,也是合成生物学重要的产业化工具。利用微生物强大且多样的生化反应网络,通过对代谢路径的重塑和工程化,可以将微生物细胞改造为能够以低价值可再生资源为原料生产各类产品的微生物细胞工厂,使底盘生物实现其特定的生物学功能。利用合成生物学方法对自然界中微生物进行改造可以提高其利用可再生生物质资源合成不同化学品的能力。也正因为这一特性,微生物细胞工厂适用于生产细胞代谢工程中的各类物质。
合成生物学与基因编辑技术包含范围不同,基因编辑技术是合成生物学改造微生物过程中使用到的技术工具之一。在生物化工产业链中,微生物细胞工厂是主要的反应单元。在改造或创制这些微生物的过程中,需要对底盘生物基因组进行“读-改-写”,使用基因“测序-编辑-合成”技术,精简、插入或重构底盘生物基因组。传统的基因编辑方法如同源重组,存在打靶效率低、操作时间长和操作繁琐等问题。为了解决这些问题,基因编辑技术从第一代锌指核酸酶(ZFN)、第二代转录激活样效应因子核酸酶(TAL effector) 发展到目前的第三代CRISPR-Cas技术。目前广泛使用的CRISPR-Cas技术具有效率高、操作快捷、效果准确等优点,是目前基因编辑的主流技术,已在多种生物体系中得到广泛应用。CRISPR技术的出现,大大提高了基因组编辑的效率,同时降低了成本,使合成生物学的盈利成为可能。
应用前景:部分替代传统化工+创造新增长空间
生物制造是传统化工的有机补充,一方面可以替代部分长流程传统生产路径,另一方面也为部分优化到极限的化学工程法打开新的研究方向,使进一步降本增效变为可能;此外,合成生物学作为新技术也在各个领域有创新性的应用场景,亟待探索。广义上而言,合成生物学产业可被界定为以生物基材料替代化石基材料、以生物技术路线替代传统化工技术路线的科技产业,是传统化工的有机补充。目前化学工程法中许多产品的工业放大装置、降本已经到达极限,市场空间平稳增长,产业急需高效低成本优质产品。未来,低碳低成本是工业发展的重要方向,合成生物学高效、低能耗、低碳、产品优质、原料可循环再生的优势符合这一趋势。目前生物制造还无法颠覆性替代传统化工,但在部分场景可以替代传统化工,尤其是一些集约程度高的长流程化学流程以及在生物代谢中能找到对应路径的产品。
从微观的原子层面来看,生物制造有能力覆盖以化石资源为基础的传统工业制造产业产品,进行替代。天然生物有 300 万种分子或新材料尚待发掘,从小分子聚合物到生物大分子再到细胞和生物材料。据麦肯锡(McKinsey)统计,生物制造的产品可以覆盖70%化学制造的产品;据波士顿咨询(BCG)预测,到21世纪末,生物制造将应用于全球1/3的制造业,有望创造30万亿美元的经济价值。根据政府“十四五”生物经济发展规划系列解读二,生物制造产业是生物经济重点发展方向,未来十年间35%的石油化工、煤化工产品将被生物制造产品替代。
实际生产中,相比化工生产,生物制造在战略与商业角度均具备优势,其原料易得、可循环,降本空间大,符合环保的经济发展方向。原料方面,生物制造的优势体现在易得与环保的特点上。传统化工生产依赖于石油、煤炭,不可再生且价格波动大,而且我国石油依赖进口,相较于生物制造的原料而言更不易得。而生物制造可使用清洁的生物质甚至CO2作为碳源,包括秸秆、玉米、高炉废气等。通过将碳源转化为糖、将糖作为生物基平台的原料基础,可以从源头解决生物制造原料和自给问题,最终产品会涵盖大宗、基础、精细、食品等领域,对目前部分传统生产体系实现大幅提升。据《中国合成生物产业白皮书2024》,生物制造当前可实现平均节能减排30%–50%,并具备未来达到50%–70%的潜力。成本方面,如同摩尔定律之于集成电路,合成生物学的“奈特定律”提出:每隔一段周期,技术的叠加会促使生物合成效率的提升、合成成本的下降。通过对菌种不断进行优化筛选,每年的副反应都会减少、转化率提升,产品生产成本降低,最终实现产品溢价。从更加长远的、环保发展战略的角度来看,生物制造过程中排出的有害物质少,推动生物制造发展也可以降低人们生产生活中对于石油基物质的依赖,缩小传统行业生产现状与未来社会发展需求在资源攫取、生产效率、安全性以及环保等方面的巨大落差,实现更多领域的可持续发展。
在实际产业落地过程中,当前化工企业纷纷布局合成生物学,产业转型升级在全球范围内已在进行中。在化工领域,合成生物学在生物基化学品的合成、生物材料、生物能源、现代农业、环境治理等领域有广泛的应用前景。近年来,合成生物学的技术进步不仅使一批合成生物学企业(例如:Ginkgo、Beam、Genomatica等)得以成长,也令许多以传统化工、医药产品开发为主的企业(例如:BASF、Dupont 等)也将目光投向合成生物学,发展生物化工,开发出一系列生物基产品。目前合成生物学可合成的大宗化学品仅几十种,在整体基础化学品中的占比还非常有限,提升空间巨大。中短期内,产业内聚焦产品开发推广的应用层公司有望通过替代化学法更快实现生产盈利;而以技术研发、服务为主的平台层、工具层公司将在合成生物学行业生态建立起来后,通过更高效专业地为大量代工企业服务获利。
合成生物学产业发展不仅将替代部分传统发酵、传统化工工业行业应用场景,也会创造新的发展空间。合成生物学产业在过去五年经历了高速增长,据据 McKinsey 数据,合成生物学市场规模从2018年的53亿美元增长到2023年的超过170亿美元,平均年增长率达27%,预计全球合成生物学市场在可见的未来仍将保持较快发展势头,将在2028年成长为体量达近500亿美元的全球型市场。
合成生物技术将在不同行业逐步完成工业化落地,应用场景逐渐打开。据《中国合成生物产业白皮书2024》,近五年内,生物制造工业化成果将主要围绕各大领域中先发探索话题的散点突破,如化学和材料中的部分基础化学品及聚合物,农业和食品中的少数食品添加剂、植物蛋白及发酵蛋白作为替代蛋白,医疗保健中创新细胞和基因疗法、部分原料药合成,以及消费品中的部分功能性小分子和重组胶原蛋白技术等;五至十年内,生物制造将围绕各大领域的应用进一步拓展,并实现部分全新子品类的技术突破和规模化生产,如材料领域的高性能蛋白、食品领域的细胞培养蛋白、农业领域的共生固氮技术、医药领域的工程菌疗法等;超过十年的远期来看,合成生物学一方面有望在热门应用领域和目前科研尚处早期/技术瓶颈较大的话题上实现工业化跑通,如活体功能材料、光合作用优化、器官再生等,另一方面,也预期将在生物质燃料、环保等新领域进一步发挥作用。
政策驱动+AI赋能:合成生物学迎来新发展阶段
合成生物学的发展随着人类对基因认知的不断深入、基因技术的不断发展、各学科交叉融合,走向应用开发与商业化的新发展阶段。科学家尝试将生物学与工程学、物理科学、计算机科学、人工智能等理论相结合,合成生物学应运而生,被视为继DNA双螺旋结构发现和人类基因组测序计划之后的第三次生物技术革命,赋能传统工业制造产业,解决人类所面临的一系列环境问题。我国在“十三五”科技创新战略规划中,已将合成生物技术列为战略性前瞻性重点发展方向。麦肯锡全球研究院( Mc-Kinsey Global Institute)发布的研究报告将合成生物学列入未来十二大颠覆性技术之一的“下一代基因组学”之中。
21 世纪以来,合成生物学领域的基础研究、应用开发、产业投资相继进入快速发展期。其发展大体经历了四个阶段:(1)创建时期(2000—2003年):产生具备领域特征的研究手段和理论,特别是基因线路工程的建立及其在代谢工程中的成功运用。(2)扩张和发展期(2004—2007 年):应用领域有扩大趋势,但工程技术进步比较缓慢。(3)快速创新和应用转化期(2008—2013 年):涌现出的新技术和工程手段使合成生物学研究与应用领域大为拓展,特别是人工合成基因组的能力提升到了接近 Mb(染色体长度)的水平,而基因组编辑技术出现前所未有的突破。(4)发展新阶段(2014 年后):工程化平台的建设和生物大数据的开源应用相结合,全面推动合成生物学技术创新以及相关应用的开发和商业化。
国内合成生物学产业目前处于部分龙头企业自发商业化获得成功、政策支持落地将近的关键时期,虽然相对海外市场起步较晚、技术方面有待积累,但在政策扶持加码、市场需求拉动、技术不断进步的推动下,国内合成生物学产业将不断开发应用场景,迎来新发展阶段。在合成生物学发展的大背景下,不同国家的生物制造产业发展呈现相似历程:技术突破—部分企业自发商业化—政策支持—建立生物制造市场。近年来,国内合成生物学公司融资加速、多家企业完成上市,产业进入快速成长期;生物制造相关政策频发,各主要省份均在加紧布局合成生物学产业集群,科研院所的发展也呈现出多点开花的态势;科技与产业的结合吸引了大量国际及国内资本对于本赛道的关注,而资本的注入正不断加速技术从实验室走向市场的进程。为成功实现商业化、促进行业发展,除了必要的政策端发力、创造机会为更多厂商提供加入市场的帮助扶持外,基础研究的持续积累不可或缺,为市场提供源源不断的新技术。
据《2024中国合成生物产业白皮书》,在上游技术方面,国内仍有多项技术亟待追赶。合成生物学技术发展可视为4个阶段循环、推动技术螺旋式进步。设计(Design)是合成生物学DBTL策略的基础,即在前期已有知识的基础上遵循一定的规则,利用现有的标准化生物元件对基因、代谢通路或基因组进行理性设计。构建(Build)过程包括DNA合成、大片段组装以及基因编辑。测试(Test)是以高效、准确和经济的检测方法从实验室中存在大量的突变体或候选目标中选择最佳生物元件及组合,以及对合成生物学DBTL整个闭环的试错性检测,高效验证DBTL过程并快速积累数据和经验。学习(Learn)涉及数据收集整合、数据分析、结果可视化和建模分析等,为下一个循环改进设计提供指导。当前组学数据大量积累以及过程检测数据剧增,专用的公共数据库为数据的收集整理提供了极大的便利。
近年来全球范围内合成生物学学科迅猛发展,人工智能(AI)的突破显著提高了合成生物学的底层研发效率,可以在短时间内分析大量数据并对生物系统进行建模、仿真,将在技术发展的4个环节赋能生物制造。AI技术可以应用于合成生物学技术开发领域,利用计算机的大数据迭代和数据库测算,在模拟软件中实现数据分析、蛋白质设计、路线设计、仿真测试等,比如对功能蛋白、功能大分子的功能特性的测试、筛选,可以显著减少前期研发步骤、筛选转化率更高的有效菌种、降低研发成本。目前人工智能(AI)技术的合成生物学应用在国内外尚处发展初期,依赖人工经验总结及学习。其中,数据分析、蛋白质结构预测及设计等尚未实现智能化,但海外在预测算法准确度、数据积累、不依赖注释预测算法等领域较为领先;在路线设计、仿真测试等合成生物学领域特有需求的技术开发方面,全球均未突破。